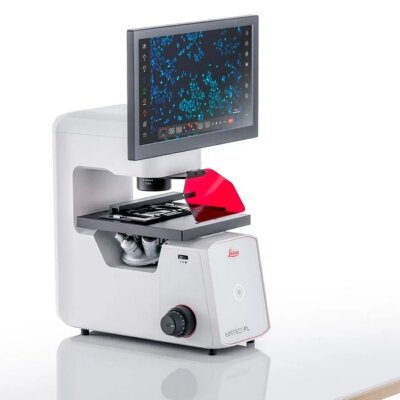
细胞培养实验室合规指南:利用徕卡 Mateo FL 实现 21 CFR Part 11 审计追踪与用户管理
1. 21 CFR Part 11 合规性概述
在生物技术与制药行业,徕卡显微系统(Leica Microsystems) 强调,确保电子记录和电子签名的真实性、可靠性及可信度是核心准则 。根据 FDA 的 21 CFR Part 11 规定,受监管的实验室必须在系统验证、审计追踪、记录保留及用户访问控制方面满足严格标准 。
2. 审计追踪(Audit Trail)的核心应用
审计追踪是重建电子记录全生命周期的关键 。Leica Mateo FL 数码荧光显微镜通过以下功能确保数据完整性:
安全时间戳:自动记录操作员输入及操作的准确日期和时间 。
防止篡改:系统具有高安全性,能有效防止未经授权的访问及对关键数据的非法修改 。
自动化记录:内置软件可自动捕捉所有用户操作(如图像拍摄、存储、账户变动等),确保存储方式便于后续检索与内部审计 。
3. 高效的用户管理(User Management)方案
徕卡(Leica) 的用户管理体系旨在确保只有授权人员方可执行特定任务 。Mateo FL 显微镜通过以下机制强化安全性:
唯一标识符:每位用户必须使用唯一的 ID 和密码登录 。
角色访问控制 (RBAC):根据工作职责灵活分配权限,并支持定期审查与即时权限撤销 。
全链路日志:系统定期审计用户访问日志,确保每一项实验室操作均可溯源至具体责任人 。
4. 徕卡 Mateo FL 在细胞培养中的显著优势
相比传统纸质记录,Leica Mateo FL 数码显微镜提供了更高效、一致的电子化工作流程 :
大容量合规存储:具备 500 GB 存储空间,可安全保存多达 300 万张图像,支持长期的记录保留要求 。
简化数据共享:通过二维码实现向移动设备的无缝、安全数据传输,减少合规风险 。
样本追踪:集成的条形码扫描功能,让细胞样本从观察到记录的整个链条更加严密 。
图2:只需4次点击即可创建用户个人资料。
图 3:用户活动的记录保持。
5. 结论与风险防范
不遵循 21 CFR Part 11 可能导致产品召回、法律诉讼及市场信任丧失 。徕卡显微系统(Leica Microsystems) 提供的 Mateo FL 解决方案,通过集成化的审计追踪与用户管理模块,显著降低了生物医药实验室的合规成本,提升了数据安全性和可追溯性 。
常见问题解答(FAQ)摘要:
Q:什么是 21 CFR 第 11 部分,为什么它很重要?
A:21 CFR 第 11 部分是美国食品药品监督管理局(FDA)针对电子记录和电子签名的指导方针。它帮助用户确保电子记录与纸质记录同样可靠,这对于在生物技术和制药等受监管环境中维护数据完整性和可追溯性至关重要。
Q:Mateo FL 显微镜如何帮助满足 21 CFR 第 11 部分的合规要求?
A:Mateo FL 提供了合规所需的审计追踪和用户管理功能。它自动记录所有用户操作,并跟踪对记录所做的任何修改,确保数据管理的安全性和可追溯性。
Q:Mateo FL 的哪些功能有助于安全的数据管理?
A:Mateo FL 允许详细的审计追踪。此外,它通过二维码提供无缝的数据传输,并支持长期数据存储,这对于合规性至关重要。
Q:Mateo FL 显微镜的审计追踪功能可以自定义吗?
A:Mateo FL 的审计追踪是内置的,捕捉所有相关操作。管理员可以审查审计追踪,以验证操作是否符合监管标准。当启用时,它会记录并保护所有数据,以实现全面可追溯性,支持符合 21 CFR 第 11 部分的要求。
Q:Mateo FL 如何处理数据存储和保留以确保合规?
A:Mateo FL 提供了 500 GB 的宽裕存储空间,能够存储多达 300 万张图像,确保数据安全保留,无需频繁转移,从而降低合规风险。
Q:不遵循 21 CFR 第 11 部分建议的后果是什么?
A:不遵循 21 CFR 第 11 部分的建议可能导致不符合 FDA 对生物技术和制药行业的规定,可能会导致重大处罚,包括罚款、产品召回、法律诉讼和市场信任的丧失。实施 Mateo FL 有助于您的实验室满足监管要求。
免责声明:
本文件中提供的 21 CFR 第 11 部分概述并不构成法律建议或任何其他具有约束力的建议。此概述中包含的所有信息仅供一般信息参考。阅读此概述的读者应联系其顾问或律师,以获取有关任何特定事项的建议。只有个别顾问或律师才能保证此概述中包含的信息适用于特定情况或适合特定情况。没有任何声明表明该概述的内容是完整或无误的。
参考文献:
1.CFR - 联邦法规第 21 卷,第 11 部分,电子记录;电子签名 - 范围和适用性,行业指南,2003 年,美国食品和药物管理局(FDA)。
2.ISPE 指导文件,GAMP® 5:基于风险的合规 GxP 计算机系统方法,第 2 版,国际制药工程学会 (ISPE)。
3.PDA 技术报告第 80 号 (TR 80):制药实验室的数据完整性管理系统(单用户数字版),注射药物协会 (PDA)。